유럽 EMA, 바이오시밀러 임상 간소화 권고 보고서 채택
비교효능임상시험 생략 가능성 열려…국내 기업 셀트리온·삼성바이오에피스에 호재
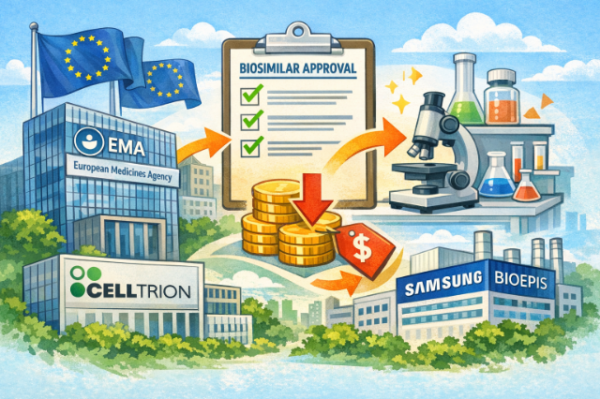
[한국유통신문= 김도형 기자] 유럽의약품청(EMA)이 바이오시밀러 임상시험 절차를 대폭 간소화할 수 있는 권고안을 공식 채택했다. 이는 글로벌 바이오시밀러 개발 전략에 중대한 변화를 예고하며, 한국 기업들에게도 긍정적 영향을 미칠 전망이다.
한국바이오협회 바이오경제연구센터에 따르면 EMA 산하 약물사용자문위원회(CHMP)는 3월 23일부터 26일까지 열린 회의에서 ‘바이오시밀러 개발에서 맞춤형 임상 접근법에 대한 성찰 보고서(Reflection paper on a tailored clinical approach in biosimilar development)’를 채택했다고 3월 27일 발표했다.
그동안 바이오시밀러 개발에는 비교성 평가를 위한 비임상시험, 약동학(PK)·약력학(PD) 시험, 비교 효능·안전성 임상시험(CES)을 모두 수행해야 했다. 그러나 EMA는 분석기술 발전과 규제 경험 축적을 바탕으로, 물리화학적·기능적 특성이 충분히 동일하게 입증된 바이오시밀러의 경우 CES가 더 이상 승인 요건이 아닐 수 있다고 밝혔다.
CHMP는 “첨단 분석 방법으로 충분히 특성화된 바이오시밀러는 제한된 임상 데이터만으로도 효능과 안전성을 담보할 수 있다”며 “이를 통해 개발 과정이 간소화될 것”이라고 결론지었다. 다만 비교 임상 PK 연구는 여전히 필수 요소로 남으며, 안전성과 면역원성 데이터는 반드시 확보해야 한다고 덧붙였다.
이번 보고서는 2024년 EU 제약 입법 프레임워크를 근거로 작성되어, 2025년 자문 및 공청회 절차를 거쳐 2026년 3월 CHMP에서 최종 의결되었다. EMA는 향후 CHMP 권고를 반영해 관련 가이드라인을 개정하고 본격 시행에 들어갈 예정이다.
2026년 3월 말 기준 EMA는 총 164개의 바이오시밀러를 승인했으며, 이 중 144개가 현재 판매 중이다. 마케팅 허가권자(MAH) 기준 상위 기업에는 셀트리온(13개)과 삼성바이오에피스(11개)가 Sandoz, STADA, Biosimilar Collaboration Ireland와 함께 포함되어 있다.
업계 관계자는 “EMA의 임상 간소화 권고는 개발 기간 단축과 비용 절감에 직접적인 영향을 미칠 것”이라며 “한국이 이미 캐나다·미국과 함께 유사한 제도 변화를 검토 중인 만큼, 글로벌 경쟁력 강화의 전환점이 될 수 있다”고 말했다.
EMA의 이번 결정은 바이오시밀러 산업 구조의 효율화를 목표로 하는 글로벌 규제 흐름과 맞닿아 있다. 한국 역시 이를 반영해 향후 임상 절차와 허가 제도의 정비를 가속화할 것으로 보인다.
<저작권자(c)한국유통신문. 무단전재-재배포 금지>
기사제보 및 사회적 공헌활동 홍보기사 문의: 010-3546-9865, flower_im@naver.com
검증된 모든 물건 판매 대행, 중소상공인들의 사업을 더욱 윤택하게 해주는
#EMA, #바이오시밀러, #바이오시밀러임상간소화, #CHMP, #유럽의약품청, #비교효능임상시험, #CES, #PK연구, #약동학, #바이오시밀러허가, #바이오시밀러개발, #바이오시밀러가이드라인, #셀트리온, #삼성바이오에피스, #K바이오, #유럽바이오시장, #바이오의약품, #규제개혁, #의약품허가, #한국바이오협회
Comments